Toen hij eind jaren negentig meldde dat er snel alzheimermedicatie zou zijn, bleek dat te voorbarig. Toch schrijft internationaal gelauwerd expert Bart De Strooper (62) in zijn nieuwe boek Tegen het vergeten dat een geneesmiddel nu niet meer veraf is.
Barbara Debusschere – De Morgen
‘De kennis is geëxplodeerd. Maar om die te verzilveren zijn maatschappelijk en politiek engagement cruciaal.’
Bart De Strooper
“Mijn moeder dementeert al jaren en ik voel me daar vaak machteloos bij”, zegt Bart De Strooper.
Want de moleculair bioloog die tot de wereldtop behoort in het alzheimeronderzoek en directeur is van het UK Dementia Research Institute had zo gehoopt dat er vandaag medicatie zou zijn.
“Twintig jaar geleden liep er veelbelovend onderzoek”, zegt hij.
“Ik dacht dat we het verval ook bij mijn moeder tijdig zouden kunnen afremmen. Dat is niet gelukt. Ze is in de mist beland.
“Als wetenschapper heb ik het daar erg moeilijk mee. Ook omdat de verzorging van dementerende mensen zoveel middelen en energie vergt van jonge mensen, alleen maar om hen in een halfbewuste toestand te houden.
“Mochten we al die dementerenden een paar jaar langer helder kunnen houden, zouden we heel veel verdriet en zorgkosten vermijden.
“We moeten veel meer inzetten op de wetenschap die de aftakeling van die hersenen probeert tegen te gaan.”
U klaagt aan dat daarover geen gevoel van urgentie is. Waarom moeten we ongeruster zijn?
“Vandaag lijden zo’n 220.000 Belgen aan dementie. Wereldwijd zijn het er 50 miljoen. Binnen dertig jaar zouden dat er drie keer meer zijn.
“Dat zijn massaal veel mensen die wegzinken en zorg nodig hebben.
“De kans is reëel dat we dat economisch en praktisch niet aankunnen en dat de enige logische reflex op een bepaald moment een euthanasieronde is.
“Dat morele dilemma wil je toch absoluut vermijden?
“Maar niemand ligt er wakker van. Je mag als wetenschapper zeggen wat je wil, de maatschappij is bezig met andere dingen. Hoe onnozeler hoe beter.
“Ook ik voel me soms als de wetenschappers in de film Don’t Look Up (waarin astronomen waarschuwen voor een komeet die op de aarde afstevent, maar velen dat negeren, BDB).
“Zonder sterke impuls vanuit de samenleving die een oplossing eist, gaat het onderzoek te traag en blijft het te kleinschalig.
“Voor kanker en aids is die maatschappelijke druk er gekomen, met onder andere Kom Op Tegen Kanker. Voor dementie is die er niet.”
Hoe komt dat?
“Door misplaatst fatalisme. We zien dementeren als een deel van ouder worden. Dat is een groot misverstand.
“De ziekte van Alzheimer is een ziekte.
“Mijn vader is gestorven aan Covid-19. Hij was 89. Maar hij was nog bij de pinken. Hij was altijd mijn grootste supporter en hij heeft gelukkig mijn boek nog gezien.
“Of neem mijn vriend en collega John O’Keefe, neurowetenschapper en Nobelprijswinnaar. Hij is vooraan in de tachtig, speelt basketbal en heeft net een boek uit.
“Kijk naar de 300 heel oude mensen die mijn Nederlandse collega Henne Holstege opvolgt sinds ze 80 zijn.
“Een van hen is 106. Die dame is nog erg lucide. Je kunt perfect ouder worden zonder te dementeren.”
Doet verouderen niet ook hersenen aftakelen?
“Heel gradueel wel, maar de wetenschap is er nog niet uit hoe veroudering de hersenfuncties impacteert. Een ouder brein zal anders werken en lost misschien iets trager een vraagstuk op, maar dat is geen dementie.
“Bij sommigen van boven de 80 zie je wel een mengvorm van veroudering en hersenziekte. Maar bij al die zestigers en zeventigers die dementeren is de reden waarom ze hun kinderen niet meer herkennen wel degelijk een specifiek ziekteproces.
“De overtuiging dat dementie nu eenmaal bij ouder worden hoort, is niet alleen fout maar ook de dood van het onderzoek. Want als het geen ziekte is hoeven we geen moeite te stoppen in een remedie.
“Iedereen die dat denkt, zou ik de hersenen van een alzheimerpatiënt willen laten zien, met daarnaast die van een gezonde leeftijdsgenoot. Dan zie je meteen hoe groot het verschil is.”
Dementie is dan weer geen ziekte?
“Inderdaad. Ook daar zit een misverstand. Dementie is een verzamelnaam voor symptomen zoals vergeetachtigheid en verwarring.
“Die symptomen zijn zoals koorts: een veruitwendiging van ziekte, in dit geval een catastrofe in het hoofd.
“Maar er zijn tientallen zo niet honderden verschillende oorzaken, van slechte doorbloeding van de hersenen tot alcoholmisbruik.
“De ziekte van Alzheimer kan er een van zijn. Wie deze ziekte heeft, heeft specifieke hersenletsels. Dat leidt vaak maar niet altijd tot dementie.”
Hoe is dat misverstand ontstaan?
“De namen van verschillende ziektes waarbij de hersencellen aftakelen zijn lastig te onthouden. Het is makkelijker om ‘dementie’ te zeggen.
“En als we dan toch een ziekte aanduiden, noemen we gemakshalve de meest bekende, de ziekte van Alzheimer.
“Maar de verwarring komt ook uit het onderzoek. Alois Alzheimer heeft in 1906 de hersenletsels bij alzheimer dan wel vastgesteld in autopsieën, lange tijd was de technologie er niet om die bij levende patiënten te zien.
“Je moest op basis van symptomen inschatten hoe waarschijnlijk het was dat iemand alzheimer had. Zo werden de symptomen gelijkgesteld aan de ziekte.
“In het onderzoek was die verwarring problematisch. Studies naar mogelijke alzheimermedicatie of -genen vergeleken een gezonde groep met een groep met dementie. Maar daarin zaten mensen die ook niet aan alzheimer leden.
“Bovendien weten we nu dat er in de gezonde groep mensen wellicht zaten die wel de alzheimerletsels hadden, maar geen dementie vertoonden. Dan krijg je misleidende resultaten.”
Maar vandaag kunnen we met hersenscans en stoffen in het bloed vaststellen wie alzheimer ontwikkelt?
“Ja, dat is een enorme vooruitgang. Idealiter kun je dat al vroeg doen, want als je dementie wil behandelen, moet je er net zoals bij kanker vroeg bij zijn.
“Wie denkt risico te lopen of symptomen te herkennen, kan zich al laten testen, onder andere met geheugentests en bloedonderzoek. Je kunt ook deelnemen aan een klinische studie, wat ook voor het grotere belang erg nuttig is.
“Tegelijkertijd is de vraag of je het als individu wel wil weten, want er is nog geen doeltreffend geneesmiddel.”
Zou u het willen weten?
“Ik heb me nog niet laten testen, maar deze ziektes zijn voor mij wel een schrikbeeld. Stel dat ik me in de toekomst vaker verward of vergeetachtig voel, dan zou ik het misschien toch doen. Want ook al is er geen medicatie, als ik weet dat ik zo’n aandoening ontwikkel, dan zou ik meer tijd met mijn familie beginnen door te brengen.”
Het gebrek aan urgentie heeft toch ook te maken met het feit dat er na grote beloftes in de jaren negentig nog geen geneesmiddel is? Velen stellen dat het onderzoek mislukt is.
“Dat klopt niet en daarom breng ik in mijn boek het volledige verhaal. Toen ik in het alzheimeronderzoek stapte stonden we nergens.
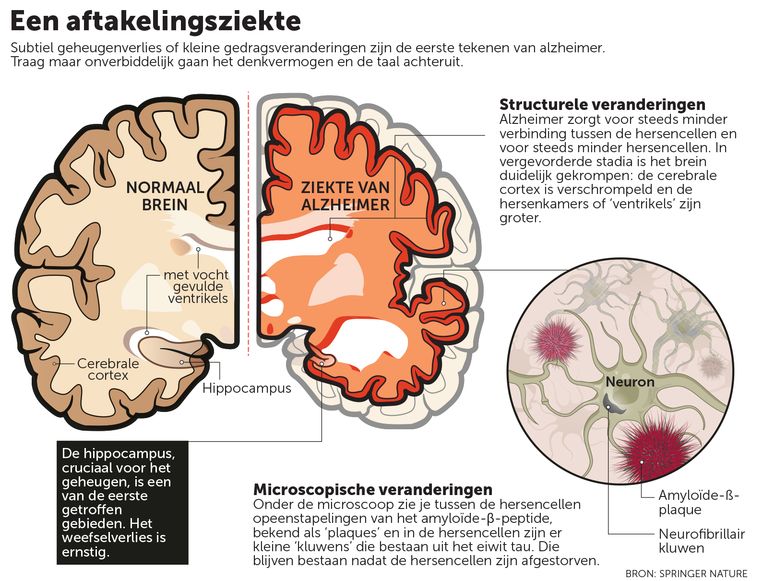
“In de jaren tachtig en negentig kwam dan een explosie van kennis. Dan is ontdekt dat de plaques en kluwens die bij alzheimer ontstaan in de hersenen bestaan uit opeenhopingen van twee specifieke soorten eiwitten.
“In 1999 publiceerde ik in Nature dat het preseniline-gen voor de neerslag van een van die eiwitten zorgt, het amyloïde-eiwit dat de ‘plaques’ rond de hersencellen veroorzaakt. Ook tau, het eiwit dat de kluwens in de hersencellen veroorzaakt, was nu bekend.
“Zeven jaar later, op de honderdste verjaardag van de ontdekking van alzheimer waren wij onder collega’s erg opgetogen omdat we op korte tijd zoveel kennis hadden vergaard.
“We dachten dat de zaak opgelost was en we binnenkort een medicijn zouden hebben.”
Nu bestempelt u die euforische verjaardag als ‘het feest van de naïviteit’ omdat het ene na het andere onderzoek met medicatie gebaseerd op de ‘amyloïdehypothese’ faalde. Is er jaren op een verkeerd spoor gezocht?
“Nee. Er waren erg goede redenen voor die hypothese. We zagen genen die ervoor zorgden dat er meer van dat amyloïde-eiwit werd aangemaakt. ‘Als we dat weghalen, halen we de ziekte weg’, was de redenering. Niet onlogisch en er is nog altijd veel van waar. Maar alzheimer bleek wel veel complexer.
“In 2017, bijna twintig jaar na die eerste Nature-paper, publiceerde ik met mijn labo dat de amyloïdeplaques niet voldoende zijn om de ziekte te veroorzaken.
“Het is hoe je hersenen erop reageren wat bepaalt of de ziekte verder evolueert.
“En die reactie wordt door je genen bepaald.
“Sommigen zijn beschermd tegen het moleculaire proces dat dan verdere aftakeling in de hersenen veroorzaakt, anderen net niet.
“Maar dit is niet het verhaal van mislukte wetenschap. Het is net normaal dat een hypothese getest, weerlegd, verfijnd wordt.
“Denk je dat het onderzoek naar kanker of aids veel sneller veel simpelere antwoorden bood? Niets is minder waar en naar die ziektes gaan veel meer onderzoeksmiddelen.
“De eerste onderzoeken naar medicatie gebaseerd op de amyloïdehypothese gaven inderdaad niet het verwachte resultaat. Men had die trials beter en diepgaander moeten herhalen en er hadden miljoenen moeten worden vrijgemaakt voor het fundamenteel onderzoek. Dan hadden we nu al veel verder gestaan.
“Maar de farma-industrie is te snel tot medicatie willen komen en is te snel afgehaakt toen het niet direct lukte.
“Niemand wil dat toegeven maar die eerste testen zijn gestart met een te klein fundamenteel begrip van die ziekte en van wat er eigenlijk werd getest.”
Door tegenvallende resultaten gaven grote farmaceuten zoals Pfizer wel de brui aan dementieonderzoek.
“Dat was een grote klap. Het is heel cynisch. Pfizer liet toen weten dat ze de draad weer zouden oppikken ‘wanneer ze nieuwe opportuniteiten zien’.
“Ze willen hun gigantische middelen dus pas weer inzetten wanneer eerst anderen de kastanjes uit het vuur halen.
“Zo ging het met Covid-19 ook. Het zijn de kleine risiconemers die het echte werk doen. Gelukkig zijn er wel nog een paar farmabedrijven die verder doen. En nu Pfizer met covid de jackpot heeft gewonnen, mogen ze wel eens in gang schieten.”
Er is dus nog geen alzheimermedicijn, maar u bent wel optimistisch. Hoe zit dat precies?
“Sinds de periode 2010-2016 is er opnieuw een exponentiële golf aan nieuwe inzichten én zijn er technologische revoluties gerealiseerd waardoor we nu veel diepgaander de biologie van de ziekte kunnen ontdekken. Onder andere de rol van ontsteking, andere soorten hersencellen en bepaalde genen wordt duidelijker.
“Momenteel testen biotechbedrijfjes zeker vijf tot tien nieuwe doelwitten voor geneesmiddelen.
“En recent heeft de FDA (de Amerikaanse geneesmiddelenwaakhond, BDB) ook een geneesmiddel goedgekeurd, Aducanumab.
“Het haalt met antilichamen de amyloïdeplaques weg. Dat kan volgens mij een kantelpunt zijn. Het vuurt risico-investeerders aan om opnieuw in de race te stappen.”
Waarom heeft Europa aducanumab dan afgekeurd?
“Omdat er onvoldoende bewijs is voor de werking ervan. De fasedrie-studies ernaar zijn vroegtijdig stopgezet omdat ze niet snel genoeg het gewenste resultaat gaven.
“Wetenschappelijk gezien zijn dit zwaluwen die mogelijk de lente aankondigen, want men ziet wel iets van verbetering. Maar dan moet je die studies opnieuw en volledig uitvoeren. Die grote investering wilde men niet maken.
“De FDA heeft dan op basis van minieme positieve effecten in die trials het middel toch goedgekeurd. Dat is politiek, een tegenzet als reactie op de grote farmabedrijven die zich terugtrokken.
“En kijk, nu al zitten drie andere antilichamen die de amyloïdeplaques verwijderen in een versnelde onderzoeksprocedure.
“Toen de FDA met diezelfde ‘speciale goedkeuringsprocedure’ in de aidscrisis van de jaren tachtig aidsmedicatie goedkeurde, was die ook niet zo effectief. Maar het heeft wellicht de weg vrijgemaakt voor snelle vooruitgang in de aidstherapie.”
U durft nu opnieuw te zeggen dat er binnen enkele jaren medicatie is?
(lacht) “Ik zou er geen exacte datum meer op plakken. Maar ik denk niet dat veel collega’s me zouden tegenspreken als ik zeg dat er medicijnen in de pijplijn zitten die elk op een ander stuk van deze complexe ziekte ingrijpen.
“Belangrijk is wel dat we heel goed verfijnen welke vorm van dementie of alzheimer iemand precies heeft. Niet elk medicijn zal voor iedereen werken. Maar het landschap ziet er veelbelovender uit dan ooit. Het zou stom zijn mochten overheden en bedrijven dat niet oppikken.
“Tegelijkertijd wil ik ook verwachtingen bijstellen. Velen willen morgen een dementiepil. Maar zo werkt het niet en zo is het ook niet gegaan met kanker.
“Dementie is minstens even complex. Dit is een proces waarin je stappen vooruitzet en de ziekte steeds beter maar niet altijd definitief of volledig leert te bedwingen.”
Waarom pleit u voor een ‘stichting’ met bijvoorbeeld als naam Tegen het Vergeten?
“Er is volgens mij een niet te negeren organisatie nodig die de nodige budgetten ophaalt en dezelfde schwung creëert als bij kanker. Alleen zo zullen we even gericht de strijd kunnen aangaan tegen een ziekte die evenveel mensen treft als kanker.
“Momenteel is dat er niet en de politiek is niet mee. Zelfs voor de EU zijn neurodegeneratieve ziekten (waarbij de hersenen aftakelen, BDB) geen prioriteit.
“Ons Fonds voor Wetenschappelijk Onderzoek heeft niet eens een aparte commissie voor onderzoek naar alzheimer en dementie.
“Als hersenwetenschapper moet je voor dezelfde jury in concurrentie met huidziekten of aandoeningen van de botten en pezen.
“Door dat gebrek aan middelen en visie leggen we ons lot in handen van de grote farmaceuten. Maar die hebben een afkeer van risico om door te zetten.
“Als ze iets ontdekken wat kankerpatiënten een paar weken langer doet leven, is daar geld en een markt voor.
“Is het een middel dat alzheimer een stukje afremt, dan wordt het meteen afgeschoten.
“We moeten uitzoeken hoe we die bedrijven motiveren wel in dit onderzoek te investeren, bijvoorbeeld door ze langer hun patent te laten behouden. Ook fundamenteel onderzoek vanuit de overheid is volgens mij essentieel.”
Wat houdt uw ‘laatste gevecht’ tegen het vergeten in?
“Tien jaar geleden dacht ik aan uitbollen, nu ben ik erg blij dat ik als directeur van het UK Dementia Research Institute het fundamenteel onderzoek mee vormgeef.
“Aan dat Britse instituut kan ik ook doorwerken tot na mijn pensioen. En met ons labo staan we in de frontlinie.
“Eén doorbraak is dat we erin slaagden om met stamcellen de biologie van alzheimer na te bootsen in muizenhersenen. We zien zo de volledige ziekte, kunnen genen aan- en uitschakelen en zo onder andere aantonen hoe hersencellen bij alzheimer precies sterven.
“Bepaalde molecules kunnen die geprogrammeerde celdood stilleggen. Mengen we die stoffen in het eten van onze muizen dan zien we na zes maanden dat we die celdood bij alzheimer kunnen stoppen. Dat maakt mijn dag goed (lacht).”
Hoe ziet de aanpak van de ziekte er in de toekomst idealiter uit?
“Dan is er medicatie die al vroeg milde dementie kan stoppen, waardoor we een heel groot deel van het sociale en maatschappelijke probleem oplossen.
“Dankzij veel beter inzicht in wat een normale hersenfunctie is, kunnen we mensen op hun dertigste, veertigste, vijftigste enzovoort screenen, zowel met scans als met cognitieve tests. Zo kunnen we op tijd ingrijpen en doelgericht medicatie geven.
“Bij ouderen met mengvormen kun je dan het alzheimeraspect behandelen met bepaalde molecules tegen alzheimer, en het parkinsonaspect met andere.”
U schetst in uw boek ook hoe uw carrière met vallen en opstaan en veel competitie begon. Hebt u advies voor jonge starters?
“Je moet vooral de juiste wetenschappers vinden die jou coachen. Dat is de startbasis. De competitie moet je erbij nemen.
“Ja, het stak toen Amerikanen mijn pluimen op hun hoed staken, maar ik heb ook toppublicaties op mijn naam.
“De kritiek op die competitie ergert me. In de sport, muziek, politiek, het bedrijfsleven is het toch niet anders?
“Hoe ouder ik word, hoe minder extreem belangrijk het is voor mij om als eerste te publiceren. Maar de competitie is wel de drijvende kracht om tot baanbrekend werk te komen.
“Als er iets moet veranderen, is dat voor mij niet de competitie, maar het academische systeem dat talent wegduwt. Het voetbal slaagt erin iedereen die talent heeft aan te trekken.
“Of je nu arm of rijk, zwart of wit bent, als je kunt voetballen ben je welkom. Maar in het wetenschappelijk onderzoek slagen we er niet in om hetzelfde te doen voor de jonge mensen met de ‘brains’.”
Hoezo?
“De manier waarop we mensen selecteren is erg eenzijdig. Ik denk niet dat ik toegang had gehad tot invloedrijke mensen die cruciaal zijn geweest om hogerop te klimmen mocht ik geen witte man geweest zijn.
“Als je toponderzoeker wil worden, moet je ook een postdoctoraat doen en dan ben je afhankelijk van beurzen.
“Na een postdoc heb je nog geen garantie op een job. Mensen die het financieel minder breed hebben, kunnen zich die risico’s niet veroorloven en vallen dan vaak af.
“Na de postdoc moet je een vaste positie zoeken. Net in de periode dat mensen typisch een gezin stichten, worden ze overladen met werk.
“Ik heb te vaak gezien hoe daardoor heel talentvolle vrouwen moesten buigen voor veel minder getalenteerde mannen. Dat is een doodzonde.
“We moeten jonge onderzoekers veel meer stabiliteit geven. Talent is veel te zeldzaam om het te laten verkwisten door zo’n ouderwets systeem. En we hebben alle talent heel hard nodig in de strijd tegen het vergeten.”

Bron: De Morgen
